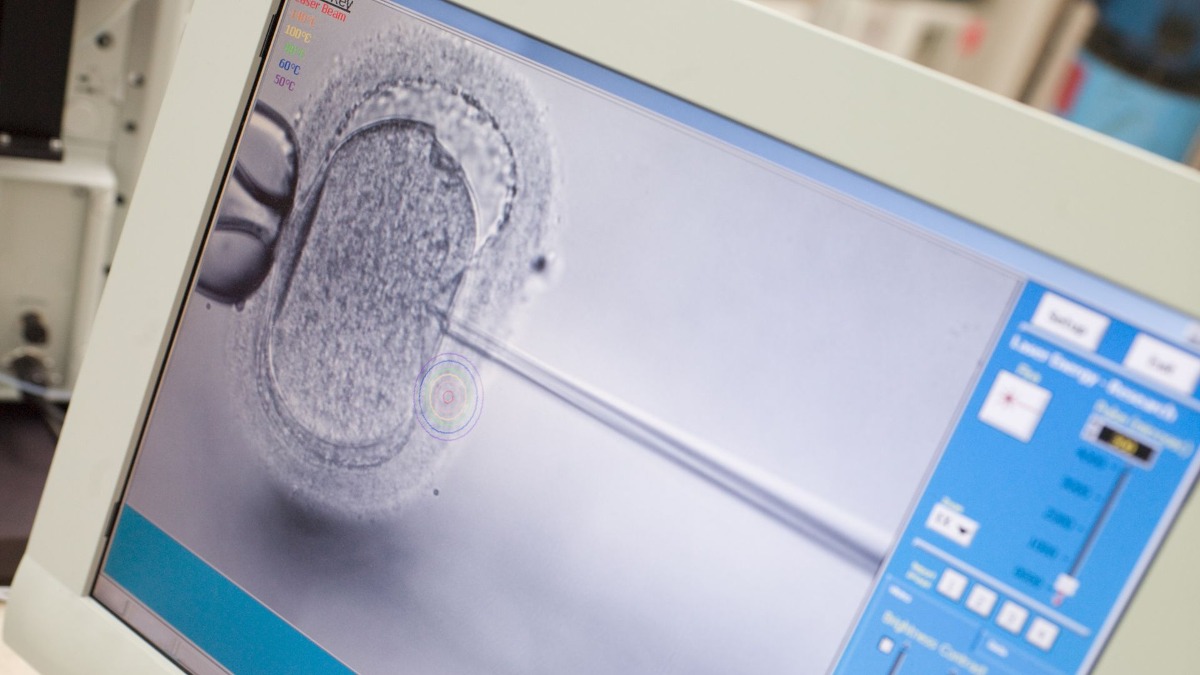
Techniques de FIV pour le traitement de l’infertilité masculine (ICSI, IMSI, MACS, PICSI, TESE) expliquées
Qu’est-ce que l’infertilité masculine ? Quels traitements de FIV ont été développés pour y remédier ?
Nombreux sont les hommes qui supposent que la capacité d’une femme à produire des ovocytes fécondables n’est pas une préoccupation qui les concerne personnellement. Pourtant, dans environ un tiers des cas d’infertilité, l’incapacité d’un couple à concevoir un enfant est due à un problème d’origine masculine, déclare Tomáš Rieger, Ph.D., embryologiste à la Gynem Fertility Clinic.

Tomáš Rieger, Ph.D., embryologiste à la Gynem Fertility Clinic
Si la femme présente également des troubles de fertilité, les chances de ne pas concevoir peuvent augmenter considérablement. Les traitements de FIV pour les femmes sont nombreux et variés, mais saviez-vous qu’une multitude de techniques de FIV ont également été mises au point pour résoudre ou atténuer les problèmes d’infertilité masculine ? Vous serez peut-être surpris et un peu perplexe, mais installez-vous confortablement, nous allons passer en revue certaines des techniques actuellement disponibles.
ICSI (Injection intracytoplasmique de spermatozoïdes)
Comme son nom l’indique, cette méthode consiste à injecter directement un seul spermatozoïde dans un ovocyte. En « allant droit au but », pour ainsi dire, cette technique augmente les chances d’une fécondation réussie lorsque le processus naturel de conception n’a pas abouti en raison de problèmes tels qu’un faible nombre de spermatozoïdes ou une absence de ceux-ci (azoospermie), une faible motilité des spermatozoïdes (vivacité !) ou une anomalie, peut-être génétique, du sperme lui-même.
La procédure
L’ICSI peut être intégrée à la procédure de FIV standard, comme suit :
- Stimulation ovarienne et prélèvement d’ovocytes : La partenaire féminine subit une stimulation hormonale pour encourager les ovaires à produire plusieurs ovocytes. Les ovocytes matures sont ensuite prélevés par une intervention chirurgicale mineure sous guidage échographique.
- Le sperme fourni par le partenaire masculin est recueilli. Si nécessaire, il peut être extrait directement des testicules – sans douleur, je m’empresse de le préciser – par une petite incision (TESE : extraction de spermatozoïdes testiculaires). Le sperme est traité en laboratoire et le spermatozoïde le plus viable (le plus sain) est sélectionné pour l’injection.
- Ce spermatozoïde « gagnant » est injecté directement dans le cytoplasme (l’intérieur) de l’ovocyte mature de la femme à l’aide d’une aiguille minuscule (une micropipette).
- Fécondation : L’ovocyte ou les ovocytes injectés sont ensuite placés dans un incubateur pour permettre la fécondation. Après la fécondation, les embryons sont cultivés (c’est-à-dire nourris et observés) pendant 3 à 5 jours, puis leur qualité est évaluée.
- Transfert d’embryon : Les embryons les plus sains sont choisis et transférés dans l’utérus de la femme. Les embryons de haute qualité restants peuvent être congelés pour une utilisation ultérieure.
- Test de grossesse : 10 à 14 jours après le transfert, un échantillon de sang est prélevé pour vérifier la grossesse.
Cela peut sembler assez simple, mais quels sont les avantages et les inconvénients ?
Avantages de l’ICSI
- Taux de réussite élevé : Comme mentionné précédemment, lorsque le problème principal est lié à des facteurs masculins tels qu’un faible nombre de spermatozoïdes ou leur absence, une faible motilité ou des spermatozoïdes endommagés, l’ICSI améliore considérablement les chances de fécondation réussie.
- Applicable aux cas sévères : L’ICSI peut être efficace même lorsque seul un petit nombre de spermatozoïdes viables est disponible.
- Contrôle de la fécondation : Comme le spermatozoïde est injecté directement dans l’ovocyte, il est épargné du périlleux voyage vers les ovaires de la femme et de la nécessité de pénétrer l’ovocyte.
- Polyvalence : L’ICSI peut être utilisée conjointement avec des ovocytes et des spermatozoïdes congelés ou décongelés, offrant une grande flexibilité dans le traitement de tout autre problème de fertilité.
Inconvénients de l’ICSI :
- Coût : L’ICSI est généralement plus onéreuse que la FIV traditionnelle en raison des compétences spécialisées requises.
- Complexité : L’expertise technique nécessaire, impliquant un équipement spécialisé, pourrait ne pas être disponible dans de nombreuses cliniques de fertilité.
- Succès non garanti : Bien que l’ICSI puisse améliorer les taux de fécondation, il n’y a aucune garantie de grossesse réussie. Le succès du traitement dépend toujours de facteurs tels que la qualité des ovocytes et des spermatozoïdes, ainsi que de l’état général de l’utérus de la femme.
Toute procédure médicale comporte un certain niveau de risque, alors quels sont les risques liés à l’ICSI ?
Risques de l’ICSI :
- Risque potentiel de malformations congénitales : Certaines études ont indiqué un risque légèrement plus élevé de malformations congénitales avec l’ICSI, bien que ces risques soient généralement faibles.
- Dommages à l’ovocyte : Le processus d’injection directe d’un spermatozoïde dans un ovocyte peut parfois endommager ce dernier, ce qui peut empêcher la fécondation ou affecter le développement de l’embryon.
- Grossesses multiples : Comme pour la FIV standard, l’ICSI peut entraîner des grossesses multiples si plusieurs embryons sont transférés, augmentant le risque de complications telles que la naissance prématurée ou un faible poids à la naissance.
- Stress physique et émotionnel : Le traitement par ICSI peut être physiquement et émotionnellement exigeant pour un couple, en particulier les traitements hormonaux impliqués dans la préparation des ovaires de la femme et le processus de prélèvement d’ovocytes. Cependant, ce type de stress n’est pas plus fréquent que dans la FIV standard et d’autres traitements de l’infertilité masculine.
Globalement, selon la Société américaine de médecine reproductive :
« L’ICSI a été associée à une augmentation des taux de fécondation et à une diminution du risque d’échec de fécondation dans certaines études… »
IMSI (Injection intracytoplasmique de spermatozoïdes morphologiquement sélectionnés) :
Ne vous laissez pas décourager par cette définition interminable. Il s’agit essentiellement de l’ICSI, mais dans une version plus sophistiquée. « Morphologiquement sélectionnés » signifie simplement que les spermatozoïdes sont choisis en fonction de leur forme et de leur structure. Avec l’IMSI, les spermatozoïdes sont soumis à un examen très détaillé au moyen d’un microscope très puissant. L’objectif est évidemment de sélectionner la « crème de la crème » des spermatozoïdes d’un homme, afin de multiplier les chances d’une fécondation réussie de l’ovocyte et d’un développement embryonnaire sain.
Avec l’IMSI, le spermatozoïde est soumis à un examen très détaillé par un microscope à très haute puissance, puis injecté dans l’ovule.
La procédure :
L’IMSI suit la même procédure générale que l’ICSI, à la différence près de l’élément « morphologique ». Nous allons donc nous concentrer sur cette étape. Voici comment cela se déroule :
- Stimulation ovarienne et prélèvement d’ovocytes
- Sperme fourni par le partenaire sélectionné
- Sélection morphologique des spermatozoïdes : À l’aide d’un microscope à fort grossissement (jusqu’à 6 000 fois, contre 200 à 400 fois pour l’ICSI standard), l’embryologiste examine rigoureusement les spermatozoïdes individuels et ne choisit que les plus aptes (en termes de forme, de taille et de structure) pour l’injection dans l’ovocyte. MSOME : Motile Sperm Organelle Morphology est l’acronyme de cette partie cruciale de la procédure.
- Fécondation
- Transfert d’embryon
- Test de grossesse : après 10 à 14 jours
Avantages de l’IMSI :
- Augmentation des chances de fécondation : En permettant aux embryologistes de choisir les spermatozoïdes de meilleure qualité, sur la base d’une morphologie détaillée, les chances de fécondation et d’amélioration de la qualité des embryons sont plus élevées.
- Amélioration des taux de grossesse : Certaines études suggèrent que l’IMSI peut conduire à des taux de grossesse et de naissance vivante plus élevés que l’ICSI standard, en particulier dans les situations d’infertilité masculine sévère ou d’échec antérieur de FIV.
- Taux de fausses couches plus bas : Une sélection améliorée des spermatozoïdes peut réduire le risque de fausse couche, car seuls les spermatozoïdes les plus sains sont utilisés.
- Utile en cas d’échecs récurrents de FIV : L’IMSI est souvent recommandée pour les couples qui ont malheureusement connu plusieurs cycles de FIV infructueux, car cette technique traite les problèmes liés aux spermatozoïdes qui peuvent être à l’origine de ces échecs.
Dans une étude publiée dans Reproductive Biology and Endocrinology par Katja Knez, Branco Zorn et al. en 2011 :
« La procédure IMSI a amélioré le développement embryonnaire ainsi que les résultats en laboratoire et cliniques de la micro-injection de sperme chez les mêmes couples infertiles souffrant d’infertilité masculine et de faible développement embryonnaire par rapport aux tentatives précédentes d’ICSI. »
Inconvénients de l’IMSI :
- Coût accru : L’IMSI peut entraîner un coût supplémentaire par rapport à l’ICSI en raison du temps d’examen supplémentaire nécessaire, du niveau d’expertise et de l’équipement (ces grossissements à 6 000 fois !) requis pour la sélection des spermatozoïdes.
- Chronophage : L’examen détaillé et l’évaluation de la morphologie des spermatozoïdes sont incroyablement laborieux, ce qui peut prolonger la durée nécessaire à la procédure. Mais, compte tenu de l’objectif final, c’est un temps qui vaut la peine d’être investi.
- 3isponibilité limitée : Une fois de plus, toutes les cliniques de fertilité ne proposent pas l’IMSI, en raison du coût et de l’acquisition d’opérateurs formés pour l’équipement.
- Aucune garantie de succès : Bien que l’IMSI puisse améliorer les chances de fécondation réussie, il n’y a aucune garantie de grossesse, d’autres facteurs, notamment la qualité des ovocytes et la santé générale de la femme, restent très importants.
MACS (tri cellulaire activé par magnétisme) :
Le MACS est une technique avancée de sélection des spermatozoïdes, spécifiquement conçue pour améliorer la qualité du sperme en séparant les spermatozoïdes sains et viables des spermatozoïdes apoptotiques, c’est-à-dire susceptibles de mourir, ou dont la structure de l’ADN est faible. Cette technique utilise des champs magnétiques pour cibler et éliminer les spermatozoïdes présentant des marqueurs indiquant une mauvaise santé, ne laissant que les plus sains pour la fécondation. Cette méthode est idéale pour les femmes présentant une faible qualité embryonnaire ou ayant subi plusieurs fausses couches, ainsi que pour les hommes chez qui on a diagnostiqué un taux élevé de fragmentation de l’ADN des spermatozoïdes. Elle peut également bénéficier aux hommes plus âgés ayant dépassé un certain âge.
La procédure :
- Stimulation ovarienne et prélèvement d’ovocytes
- Recueil du sperme : Le sperme est recueilli par éjaculation ou, si nécessaire, directement à partir des testicules à l’aide d’une procédure telle que la TESE (extraction de spermatozoïdes testiculaires).
- Tri des spermatozoïdes par MACS :
- Marquage des spermatozoïdes apoptotiques : Le sperme recueilli est d’abord incubé avec un réactif (Annexine V), une protéine qui se lie à la phosphatidylsérine, un marqueur de l’apoptose.
- Le sperme traité est passé à travers un filtre magnétique. Les cellules marquées restent dans le filtre et les spermatozoïdes sains le traversent et sont recueillis.
- Une fois recueillis, les spermatozoïdes sont ensuite préparés pour leur tâche de fécondation
- Fécondation : Ces spermatozoïdes de haute qualité sont utilisés pour féconder les ovocytes prélevés, soit par FIV standard, où les spermatozoïdes et les ovocytes sont incubés ensemble, soit par ICSI, détaillée ci-dessus.
- Culture embryonnaire : Les ovocytes fécondés sont cultivés pendant 3 à 5 jours.
- Transfert d’embryon : Les embryons de meilleure qualité sont sélectionnés et transférés dans l’utérus de la femme.
- Test de grossesse : Après 10 à 14 jours.
Avantages du MACS :
- Une sélection améliorée de spermatozoïdes et d’embryons de haute qualité
- Il y a, potentiellement, une réduction des taux de fausses couches.
- La procédure améliore également potentiellement le taux de réussite dans les cycles de FIV.
- Elle peut contribuer à la formation et au développement sains des embryons.
Inconvénients du MACS :
- Une fois encore, toutes les cliniques de fertilité ne sont pas en mesure de s’offrir l’équipement coûteux nécessaire, et le traitement peut s’avérer onéreux pour les couples.
- La naissance n’est pas garantie, bien que cela s’applique à la plupart des traitements de FIV et de fertilité masculine.
Une étude récente de 2020, menée par Alberto Pacheco, Arancha Blanco et al., publiée dans The Journal of Clinical Medicine, a conclu que :
« La sélection des spermatozoïdes humains par MACS est une méthode sûre, facile et appropriée pour la préparation du sperme en vue d’une utilisation en ICSI dans un contexte clinique. Les résultats présentés dans cette étude indiquent que la technique de sélection MACS pourrait contribuer à améliorer les résultats en matière de reproduction… »
PICSI (Injection intracytoplasmique de spermatozoïdes physiologiquement sélectionnés) :
La PICSI est une variante de l’ICSI standard (voir ci-dessus), mais elle l’améliore en utilisant une méthode qui sélectionne les spermatozoïdes selon leur capacité à se lier à l’acide hyaluronique, une substance chimique naturellement présente dans la couche externe de l’ovocyte féminin. Les spermatozoïdes capables de s’attacher à l’acide hyaluronique sont généralement plus matures, génétiquement plus robustes et cohésifs, améliorant ainsi les taux de fécondation et la qualité des embryons. La PICSI peut être recommandée pour les hommes présentant un taux élevé de fragmentation de l’ADN spermatique ou pour les couples confrontés à une forme inexpliquée d’infertilité. Elle est également préconisée en cas de fausses couches à répétition, d’échecs antérieurs de FIV ou pour les couples ayant connu plusieurs tentatives infructueuses de FIV.
La procédure :
- Stimulation ovarienne et prélèvement d’ovocytes.
- Recueil du sperme du partenaire masculin : par éjaculation ou TESE.
- Sélection des spermatozoïdes par PICSI :
- Liaison à l’acide hyaluronique (HAB) : le sperme est déposé dans une boîte spéciale recouverte d’un gel d’acide qui reproduit l’environnement de la couche externe d’un ovocyte.
- Sélection des spermatozoïdes matures : seuls les spermatozoïdes dotés de récepteurs pour l’acide se lieront au gel – ceux présentant moins d’anomalies chromosomiques et de fragmentation de l’ADN. Les spermatozoïdes liés sont ensuite sélectionnés pour l’étape suivante.
- Procédure ICSI : ces spermatozoïdes plus sains sont adaptés pour une injection directe dans le cytoplasme des ovocytes matures en utilisant la procédure ICSI standard (détaillée ci-dessus).
- Culture embryonnaire : Les ovocytes fécondés sont cultivés pendant 3 à 5 jours.
- Transfert d’embryons : Les embryons de meilleure qualité sont sélectionnés et transférés dans l’utérus de la femme.
- Test de grossesse : Après 10 à 14 jours.
Avantages de la PICSI :
- Amélioration de la sélection des spermatozoïdes.
- Taux de fécondation et de grossesse plus élevés.
- Risque réduit d’anomalies génétiques chez les embryons résultants : les spermatozoïdes sélectionnés par PICSI ont plus de chances d’avoir une structure chromosomique normale en raison de leur meilleure qualité.
- Taux de fausses couches plus bas : certaines études suggèrent que la PICSI contribue à réduire les taux de fausses couches.
- Un processus de sélection plus naturel : la PICSI imite un processus de sélection naturel en s’appuyant sur la capacité des spermatozoïdes à se lier à l’acide hyaluronique.
Inconvénients de la PICSI :
- Coût accru : la PICSI est généralement plus onéreuse que l’ICSI standard en raison des étapes supplémentaires et de l’équipement spécialisé nécessaire à la sélection des spermatozoïdes.
- Disponibilité limitée : Toutes les cliniques de fertilité ne proposent pas la PICSI, en raison des coûts et de l’expertise spécialisée requise, bien qu’il existe des cliniques spécialisées qui offrent cette procédure.
- Aucune garantie de succès : La PICSI peut améliorer les chances de fécondation et d’obtention d’un embryon sain, mais bien entendu, comme nous l’avons déjà établi, la grossesse ne peut être garantie avec aucune procédure.
- Chronophage : Les étapes supplémentaires nécessaires avec la PICSI peuvent allonger le processus de FIV.
Une étude menée en 2020 par Roisin Ni Dhuifin et Darren K. Griffin et al., publiée dans DNA, a conclu que :
« Bien qu’il y ait peu de preuves suggérant que la sélection des spermatozoïdes par HAB améliore les taux de fécondation ou de naissances vivantes, cette technique améliorerait l’incidence des pertes de grossesse après AMP (Assistance Médicale à la Procréation) dans une population d’infertilité non sélectionnée. » Cependant, les chercheurs admettent que « les résultats de cette étude sont probablement influencés par la faible qualité des études. »
TESE, MESA :
Nous avons déjà mentionné les deux premiers de ce trio au nom évocateur, mais comme ils sont étroitement liés, examinons-les ensemble.
La TESE (Extraction de spermatozoïdes testiculaires) et la MESA (Aspiration microchirurgicale de spermatozoïdes épididymaires) sont des procédures chirurgicales utilisées pour prélever des spermatozoïdes directement dans les testicules ou l’épididyme en cas d’infertilité masculine, notamment lorsqu’il n’y a pas de spermatozoïdes dans l’éjaculat (azoospermie) ou lorsque les spermatozoïdes ne peuvent être récupérés par des moyens plus conventionnels. L’azoospermie est associée à 20 % des cas d’infertilité masculine et peut constituer un véritable obstacle à une FIV efficace.
Comme nous l’avons vu précédemment, ces procédures sont couramment utilisées en tandem avec l’injection intracytoplasmique de spermatozoïdes (ICSI) dans les cycles de FIV.
TESE : Cette procédure consiste à pratiquer une petite incision dans les testicules et à extraire directement de petites quantités de tissu testiculaire, à partir desquelles les spermatozoïdes peuvent ensuite être isolés.
MESA : Ici, les spermatozoïdes sont prélevés dans l’épididyme, un tube enroulé où les spermatozoïdes arrivent à maturité et sont stockés, en utilisant des techniques microchirurgicales.
La procédure :
La TESE et la MESA sont généralement réalisées lorsque le partenaire masculin présente une azoospermie obstructive ou non obstructive. Elles sont habituellement effectuées en ambulatoire sous anesthésie locale, sédation ou anesthésie générale. Voici comment elles s’intègrent dans le processus de FIV/ICSI :
- Stimulation ovarienne et prélèvement d’ovocytes (partenaire féminine) : La partenaire féminine subit une stimulation ovarienne pour produire plusieurs ovocytes, qui sont prélevés par une intervention chirurgicale mineure.
- Prélèvement de spermatozoïdes (partenaire masculin):
- TESE : Après administration de l’anesthésie, le chirurgien pratique une petite incision dans le scrotum et le testicule pour accéder au tissu testiculaire. De petites biopsies sont réalisées et les spermatozoïdes sont extraits de ces échantillons de tissu.
- MESA : À l’aide d’un microscope chirurgical, le chirurgien ouvre soigneusement l’épididyme et aspire le liquide contenant les spermatozoïdes. Cette méthode est souvent utilisée lorsqu’il y a une obstruction empêchant les spermatozoïdes d’entrer dans l’éjaculat.
- Traitement des spermatozoïdes : Les spermatozoïdes prélevés sont traités et évalués en laboratoire. Si des spermatozoïdes viables sont trouvés, ils sont préparés pour l’injection dans les ovocytes.
- Procédure ICSI : Les spermatozoïdes prélevés sont injectés directement dans le cytoplasme des ovocytes récupérés, augmentant ainsi la probabilité de fécondation.
- Fécondation et culture embryonnaire.
- Transfert d’embryons
- Test de grossesse : Environ 10 à 14 jours après le transfert d’embryons pour confirmer la grossesse.
Avantages, inconvénients et risques des procédures TESE et MESA
TESE (Extraction de spermatozoïdes testiculaires)
Avantages :
- Prélèvement direct de spermatozoïdes : La TESE permet l’extraction de spermatozoïdes directement à partir du tissu testiculaire, ce qui peut être crucial pour les hommes atteints d’azoospermie (absence de spermatozoïdes dans l’éjaculat).
- Utile pour l’azoospermie non obstructive : Elle est particulièrement efficace dans les cas d’azoospermie non obstructive où la production de spermatozoïdes est altérée mais pas complètement absente.
- Possibilité de production de spermatozoïdes : La TESE peut identifier des zones dans le tissu testiculaire où la production de spermatozoïdes est en cours, même dans les cas de très faible numération spermatique.
Inconvénients :
- Procédure invasive : La TESE nécessite une petite incision dans le scrotum, ce qui peut entraîner un inconfort postopératoire et un temps de récupération plus long par rapport à des méthodes moins invasives.
- Rendement en spermatozoïdes plus faible : La procédure peut produire un nombre limité de spermatozoïdes viables, en particulier dans les cas d’insuffisance spermatogénique sévère.
Risques :
- Infection : Comme pour toute procédure chirurgicale, il existe un risque d’infection au niveau du site d’incision.
- Saignement et hématome : Il y a un risque de saignement ou de formation d’un hématome (caillot sanguin) dans le scrotum.
- Cicatrisation : L’incision peut entraîner une cicatrisation qui pourrait potentiellement affecter la fonction testiculaire ou la fertilité future.
MESA (Aspiration microchirurgicale de spermatozoïdes épididymaires)
Avantages :
- Prélèvement de spermatozoïdes de haute qualité : La MESA est efficace pour obtenir des spermatozoïdes de haute qualité de l’épididyme, ce qui peut être bénéfique pour la FIV/ICSI.
- Moins invasive que la TESE : La MESA est moins invasive que la TESE et implique l’utilisation de techniques microchirurgicales pour accéder à l’épididyme par de petites incisions.
Inconvénients :
- Nécessite des compétences spécialisées : La MESA requiert des compétences microchirurgicales spécialisées et un équipement qui peut ne pas être disponible dans tous les centres de fertilité.
- Risque de formation de tissu cicatriciel : Des procédures répétées peuvent entraîner la formation de tissu cicatriciel, affectant potentiellement les futurs prélèvements de spermatozoïdes.
Risques :
- Risques chirurgicaux : Comme pour toute procédure chirurgicale, il existe des risques d’infection, de saignement et de complications liées à l’anesthésie.
- Impact à long terme : Il existe un risque potentiel d’effets à long terme sur l’épididyme, ce qui pourrait avoir un impact sur le transport des spermatozoïdes et la fertilité future.
Le NHS (National Health Service) au Royaume-Uni a conclu en 2016 qu’
« il existe suffisamment de preuves pour soutenir une proposition de mise en œuvre systématique de la MESA pour les hommes atteints d’azoospermie obstructive et de la TESE pour les hommes atteints d’azoospermie non obstructive afin de faciliter la conception. »
SpermMobil dans le traitement par FIV
Ce nom un peu étrange fait référence à un milieu spécialisé utilisé pour améliorer la motilité des spermatozoïdes dans les cas d’infertilité masculine. Il est conçu pour améliorer le mouvement des spermatozoïdes, les rendant plus aptes à atteindre et à féconder les ovocytes. SpermMobil est une solution unique qui optimise l’environnement pour la motilité et la fonctionnalité des spermatozoïdes. Il est particulièrement utile dans les cas où les spermatozoïdes ont une faible motilité, ce qui peut avoir un impact significatif sur les taux de fécondation. De plus, pour les hommes ayant subi des procédures de prélèvement de spermatozoïdes comme la TESE, SpermMobil peut optimiser la motilité des spermatozoïdes prélevés. Le Docteur Tomáš Rieger de la clinique Gynem est enthousiaste :
« SpermMobil est un milieu qui contient de la théophylline et d’autres constituants qui, pendant une courte période, accélèrent le mouvement des spermatozoïdes autrement immobiles. Ce sérum est généralement utile lorsque le sperme a été extrait chirurgicalement du testicule (TESE) car certains spermatozoïdes peuvent bouger très peu, voire pas du tout, mais conservent la santé et la capacité de produire un bébé. L’effet énergisant de SpermMobil peut donc nous aider à identifier les spermatozoïdes lents, mais toujours vivants et viables pour le traitement ICSI. En utilisant ce milieu, nous pouvons éviter le risque de négliger des spermatozoïdes sains simplement parce qu’ils semblent morts à première vue. »
La procédure :
- Stimulation ovarienne et prélèvement d’ovocytes
- Recueil du sperme : Le sperme est recueilli auprès du partenaire masculin. Dans les cas d’infertilité masculine sévère, les spermatozoïdes peuvent être extraits directement des testicules ou de l’épididyme à l’aide de procédures comme la TESE ou la MESA.
- Préparation du sperme avec SpermMobil :
- Traitement du sperme : Le sperme recueilli est mélangé avec SpermMobil, un milieu conçu pour améliorer la motilité des spermatozoïdes. Ce milieu fournit des nutriments et un environnement favorable qui aide à améliorer le mouvement des spermatozoïdes.
- Amélioration de la motilité : SpermMobil optimise la capacité des spermatozoïdes à nager et à se déplacer efficacement, augmentant ainsi leurs chances d’atteindre et de féconder l’ovocyte.
- Procédure ICSI : Les spermatozoïdes améliorés, préparés avec SpermMobil, sont ensuite utilisés dans la procédure d’injection intracytoplasmique de spermatozoïdes (ICSI). Un seul spermatozoïde lavé est injecté directement dans le cytoplasme de l’ovocyte pour faciliter la fécondation.
- Fécondation et culture embryonnaire : Après l’injection, les ovocytes sont mis en culture pour permettre la fécondation et le développement embryonnaire. Les embryons sont surveillés pour évaluer leur qualité et leur développement.
- Transfert d’embryons : Les embryons de meilleure qualité sont sélectionnés et transférés dans l’utérus de la femme. Les embryons viables restants peuvent être congelés pour une utilisation future.
- Test de grossesse : Environ 10 à 14 jours après le transfert d’embryons pour confirmer la grossesse.
Avantages, inconvénients et risques
Avantages :
- Amélioration de la motilité des spermatozoïdes : SpermMobil améliore le mouvement des spermatozoïdes, ce qui peut être particulièrement bénéfique dans les cas de faible motilité spermatique (asthénozoospermie).
- Augmentation des taux de fécondation : En optimisant la motilité des spermatozoïdes, SpermMobil peut améliorer les chances de fécondation réussie, conduisant à des taux de grossesse plus élevés.
- Environnement favorable : Le milieu utilisé dans SpermMobil fournit un environnement propice aux spermatozoïdes, améliorant potentiellement leur fonctionnalité globale.
Inconvénients :
- Pas une solution autonome : SpermMobil n’est pas un remède à tous les problèmes d’infertilité masculine ; il vise spécifiquement à améliorer la motilité des spermatozoïdes et peut ne pas traiter d’autres causes sous-jacentes d’infertilité.
- Coût supplémentaire : L’utilisation de milieux spécialisés comme SpermMobil peut augmenter le coût global du traitement FIV.
Traitements hormonaux pour l’infertilité masculine
Il existe également certains médicaments qui peuvent être utilisés pour traiter les déséquilibres hormonaux susceptibles d’affecter la production et la qualité des spermatozoïdes.
La procédure :
Les traitements hormonaux sont prescrits en fonction de diagnostics spécifiques, tels que de faibles niveaux de testostérone (hypogonadisme) ou d’autres problèmes hormonaux affectant la production de spermatozoïdes.
Avantages :
- Peut améliorer le nombre et la qualité des spermatozoïdes dans les cas où des déséquilibres hormonaux sont identifiés
- Approche non chirurgicale pour traiter certains problèmes d’infertilité.
Inconvénients :
- L’efficacité varie en fonction de la cause sous-jacente de l’infertilité.
- Peut nécessiter un suivi continu et des ajustements.
Risques :
- Effets secondaires possibles des médicaments hormonaux.
- Les traitements hormonaux peuvent ne pas résoudre tous les problèmes de fertilité.

Un mode de vie malsain—le tabagisme, un stress élevé et la restauration rapide—peut nuire à la santé des hommes, affecter la fertilité et réduire la qualité du sperme.
Mieux vaut prévenir que guérir ?
Il y a certainement une part de vérité dans ce vieux proverbe. Des études récentes menées dans le monde entier confirmant que les habitudes de la vie moderne peuvent réduire le nombre et la qualité des spermatozoïdes masculins, il est judicieux pour les hommes de prendre soin de leur santé, car la fertilité masculine – ou spermatogenèse – peut être améliorée par un mode de vie sain. Voici quelques domaines sur lesquels nous pouvons tous nous pencher :
- Tabagisme : arrêtez si vous le pouvez, réduisez si vous ne pouvez pas, car les fumeurs accumulent des métaux lourds dans leur organisme qui inhibent le travail de réparation effectué par notre ADN.
- Réduire la consommation d’alcool : l’alcool affecte négativement le fonctionnement de l’hypophyse, qui régule les hormones impliquées dans la spermatogenèse.
- Drogues récréatives : il existe de meilleures formes de loisirs, messieurs : le tennis, le football, la salle de sport, par exemple.
- Stress et manque de sommeil : trouvez des moyens, tels que la pleine conscience, la méditation ou simplement une promenade tranquille dans la nature, pour réduire le stress et améliorer les habitudes de sommeil. Le manque de sommeil et le stress ont un impact direct sur la production de testostérone.
- Obésité : le surpoids a des impacts négatifs sur la santé de tout votre organisme.
Nous pouvons également favoriser notre fertilité en nous rendant à la pharmacie et en nous offrant quelques
- vitamines et compléments alimentaires tels que : Vitamine C, B12, Zinc, Sélénium, Vitamine D, Folate, Acétyl Coenzyme Q10.
- Plantes : Anémone pulsatille, Millepertuis, Ginseng à deux lobes.
Nous espérons que cet article vous a aidé à prendre la bonne décision de traitement sur votre chemin pour devenir père. Si vous avez d’autres questions sur l’une des techniques mentionnées ci-dessus, nous vous recommandons de consulter un spécialiste de l’infertilité masculine à la Gynem Fertility Clinic.
Liens :
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3922320/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10185595/
https://academic.oup.com/jcem/article/82/3/709/2656193
https://www.sciencedirect.com/topics/medicine-and-dentistry/in-vitro-fertilisation